迈威生物,下一个 Biotech 盈利新星?
医药市场波谲云诡,无数 Biotech 企业都在试图从白热化的竞争中脱颖而出。然而,迈威生物却以半年涨幅高达 150%,成为资本市场 “最靓的仔”。
近日,迈威生物公布 2023 年财报:实现总营收 1.28 亿元,同比激增 361.03%,再次被推至市场聚光灯下。
然而,面对激烈的市场竞争,迈威生物能否保持强劲的发展势头?其研发的创新药又能否成功 ‘出海’,成为公司扭亏为盈的关键?这些都是市场关注的焦点。
01
商业化产品增至 3 款,
全面覆盖多个治疗领域
“生物类似药先行” 策略,得到了市场的正反馈。
2023 年,迈威生物迎来了 “蜕变”:实现总营收 1.28 亿元,主要来自技术服务收入 8559.5 万元和药品销售收入 4209 万元,比去年同期增长 361.03%。
其中,技术服务收入主要系 9MW3011 项目与美国 DISC MEDICINE,INC.达成独家许可协议并收到其支付的不可退还的首付款 1000 万美元;药品销售收入,来自两款商业化产品君迈康和迈利舒的销售。
9MW3011是迈威生物全球首创的抗 TMPRSS6 单抗,针对包括β-地中海贫血、真性红细胞增多症等与铁稳态相关的罕见病,目前这些适应症尚无成熟有效的大分子治疗药物。
2023 年 1 月,迈威生物将 9MW3011 除大中华区和东南亚以外所有区域内的独家权益授予 Disc 公司,将获得合计最高达 4.125 亿美元的首付款及里程碑付款(其中首付款 1000 万美元),以及产品净销售额最高近两位数百分比的特许权使用费。
值得一提的是,在与 Disc 公司合作后,9MW3011 先后获得 FDA 授予快速通道认定和孤儿药资格认定,用于治疗真性红细胞增多症。这意味着,9MW3011 未来有望加快上市速度,且能享受到临床费用减免、七年市场独占权等政策优惠。
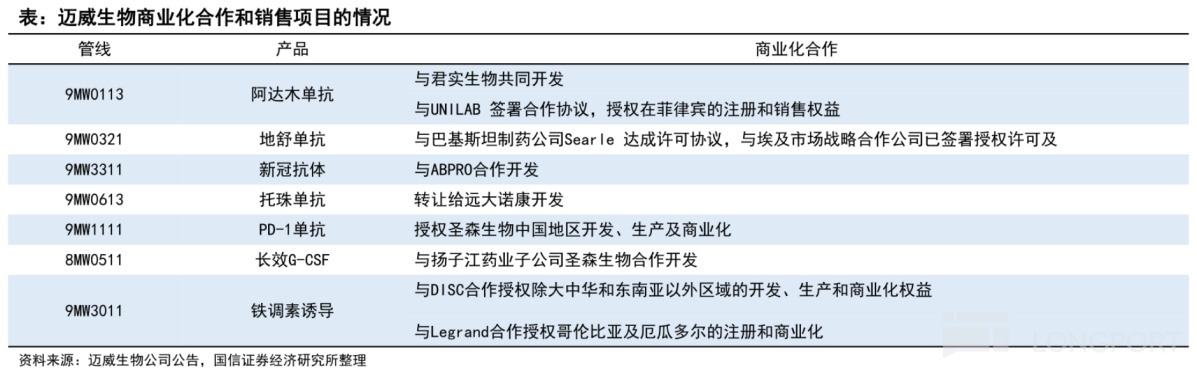
已上市产品中,君迈康(阿达木单抗生物类似药)、迈利舒(项目代码:9MW0311)分别于 2022 年 3 月、2023 年 3 月获批上市。
其中,迈利舒是全球第 2 款获批上市的普罗力(地舒单抗,Prolia)生物类似药,用于骨折高风险的绝经后妇女的骨质疏松症,后续拟递交补充申请,增加骨折高风险的男性骨质疏松症适应症。
尽管迈利舒已抢得一定的先发优势,但仍面临不小的竞争压力,目前已获批上市的同类竞品还有博安生物的博优倍、齐鲁制药的鲁可欣,而且石药集团 JMT103、康宁杰瑞/菲洋生物的 KN012 均已开展Ⅲ期临床。
面临竞争与业绩压力,必然需要寻找新的增长点,以提升盈利能力。
今年 4 月,迈卫健(项目代码:9MW0321)获国家药监局批准上市,用于治疗不可手术切除或者手术切除可能导致严重功能障碍的骨巨细胞瘤,包括成人和骨骼发育成熟(定义为至少 1 处成熟长骨且体重≥45kg)的青少年患者,成为我国首款获批上市的安加维(地舒单抗注射液,120mg)生物类似药。
从市场格局看,原研药安加维于 2019 年在中国上市,2022 年销售额为 4.27 亿元。生物类似药方面,齐鲁制药、博安生物已提交上市申请,石药集团、豪森药业和华兰基因已开展Ⅲ期临床,竞争十分激烈。
这意味着,迈威生物虽在肿瘤、自免和代谢领域已有生物类似药获批上市,商业化产品增至 3 款,但若想填补大规模的研发支出还远远不够。
02
另辟蹊径 “出海”,
新兴市场成 “必争之地”
由于生物类似药天然存在市场竞争激烈的基因,取胜的关键不仅在于速度,还得有另辟蹊径的销售策略。
尤其国内市场竞争激烈,“出海” 成为了 “必答题”。
基于此,包括迈威生物在内的一些布局生物类似药的药企,选择将产品对外授权、实现 “借船出海”,且逐渐转向新兴市场,而非主流的欧美市场。
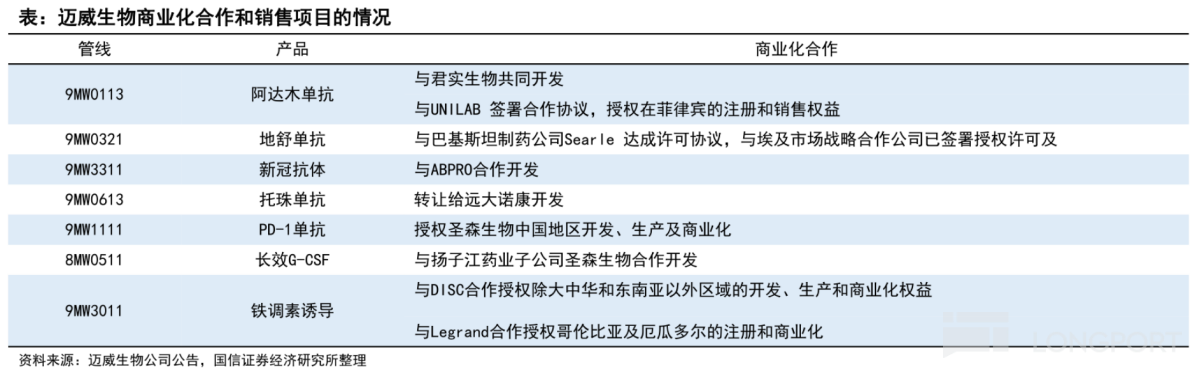
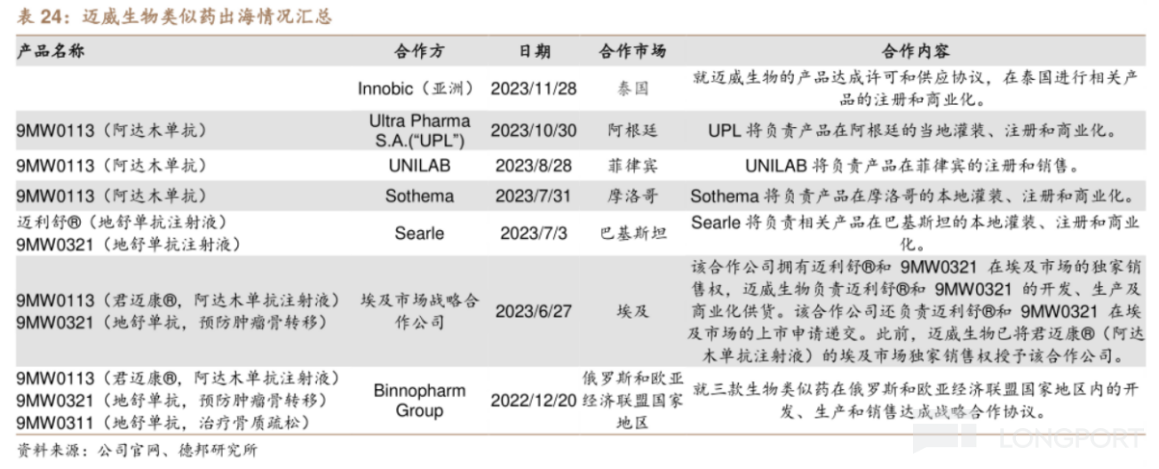
例如,与迈威生物阿达木单抗生物类似药达成授权合作的海外药企颇多,包括摩洛哥最大制药集团 Sothema、东盟制药行业位列第一的 UNILAB 和 UPL 公司,且辐射的版图也较多,包括摩洛哥、菲律宾、阿根廷、俄罗斯和欧亚经济联盟国家地区。
另外,迈威生物还针对9MW0311(普罗力生物类似药)和9MW0321(安加维生物类似药)与巴基斯坦、埃及、泰国、印尼、哥伦比亚、厄瓜多尔等 6 个国家签署正式协议,以及与印度制药公司达成供应和商业化协议,后者可获得9MW0813(阿柏西普生物类似药)在印度进口、生产、注册、上市和销售的独家权利,并有权获得包括南亚及非洲部分国家在内的 10 个国家的非独家权利。
截至 2023 年财报披露日,迈威生物已完成覆盖海外市场数十个国家的正式协议或框架协议的签署,并已向印尼、埃及、巴基斯坦等国家递交注册申请文件,不断攻城略地。
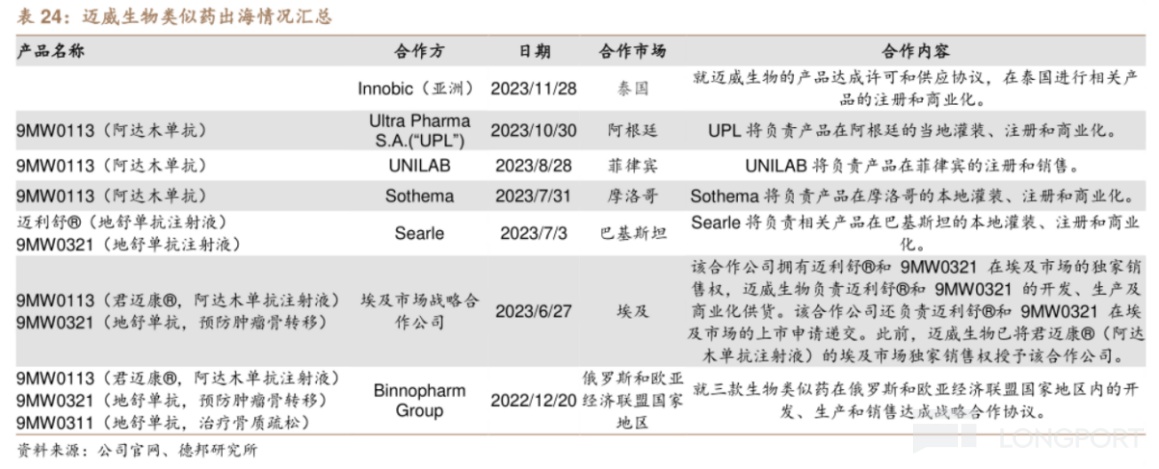
实际上,不仅仅是迈威生物,这两年包括百奥泰、复宏汉霖等国内药企,也将产品出海的方向拓展至新兴市场。
毕竟,相比欧美等成熟市场,新兴市场的竞争压力相对较小、进入门槛相对较低,且对于价格适中的药物有着更为迫切的需求,药企可以更容易地获得市场份额和建立品牌知名度。
可见,新兴市场及 “一带一路” 沿线国家已成为中国药企 “出海” 的必争之地。
03
10 个创新药在研,
多款具备出海潜质
除另辟蹊径 “出海” 外,迈威生物在管线研发上也有着不少亮点。
作为一家创新型生物医药企业,迈威生物一直保持高额研发投入,最近三年分别为 6.23 亿元、7.59 亿元、8.36 亿元。尽管使得亏损额逐年扩大,但也布局了许多进度处全球前列的创新药,尤其 3 款差异化 ADC 管线具备出海潜质。
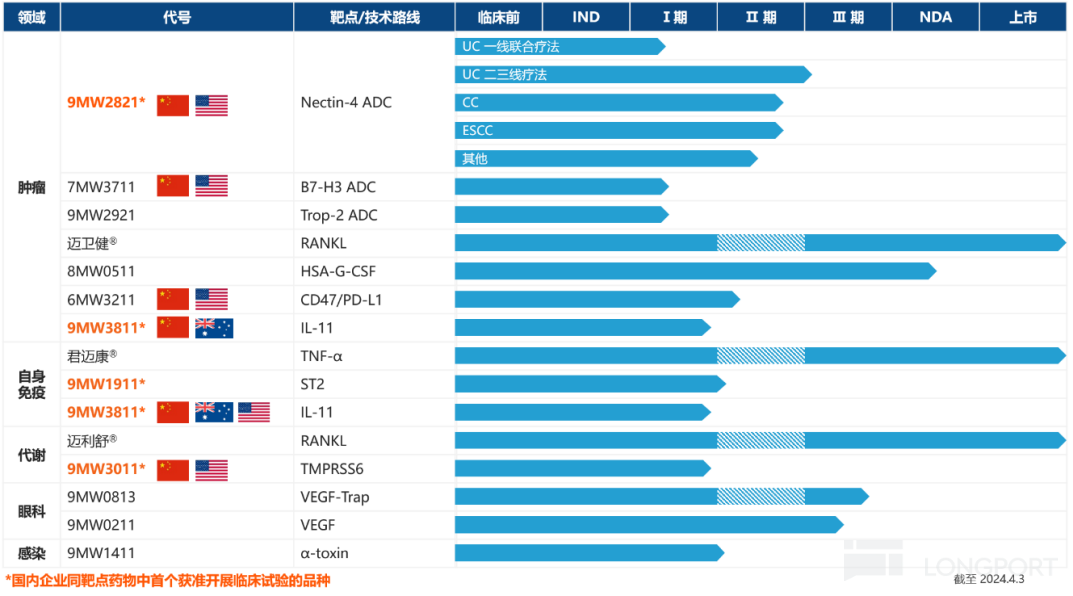
截至 2023 年财报披露日,迈威生物共拥有 14 个处于临床或上市阶段的品种,包括 10 个创新药,4 个生物类似药,覆盖自身免疫、肿瘤、代谢、眼科、感染等多个治疗领域。其中,已上市品种 3 个,处于上市许可审评阶段品种 1 个,处于 III 期关键注册临床阶段品种 3 个,处于其他不同临床阶段品种 7 个。
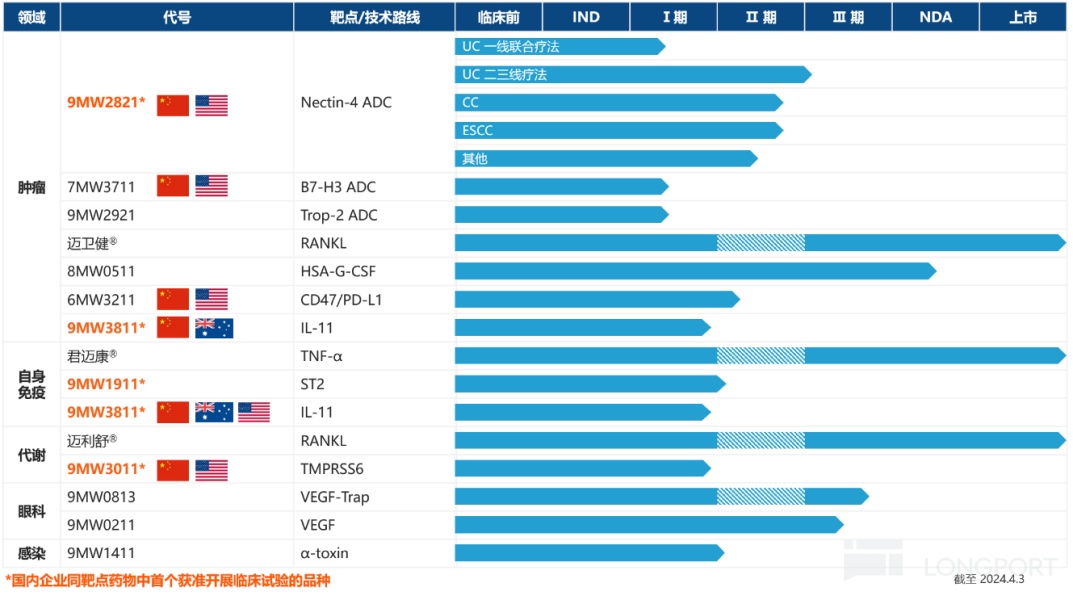
迈威生物研发管线
图源:2023 年财报
在 2023 年财报中,迈威生物明确表示:将重点针对创新度较高且差异化优势明显的管线推进国际合作,包括靶向Nectin-4 ADC(9MW2821)、靶向 B7-H3 ADC(7MW3711)、抗 ST2 单抗(9MW1911)、抗 IL-11 单抗(9MW3811)等管线。
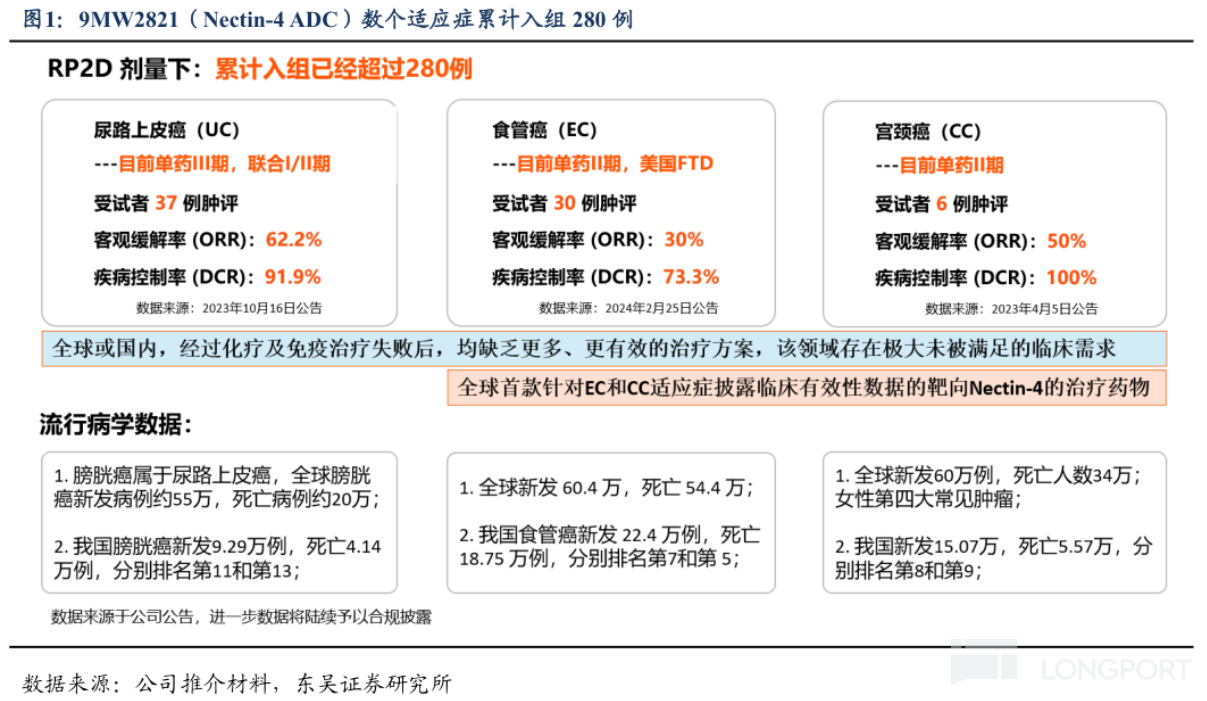
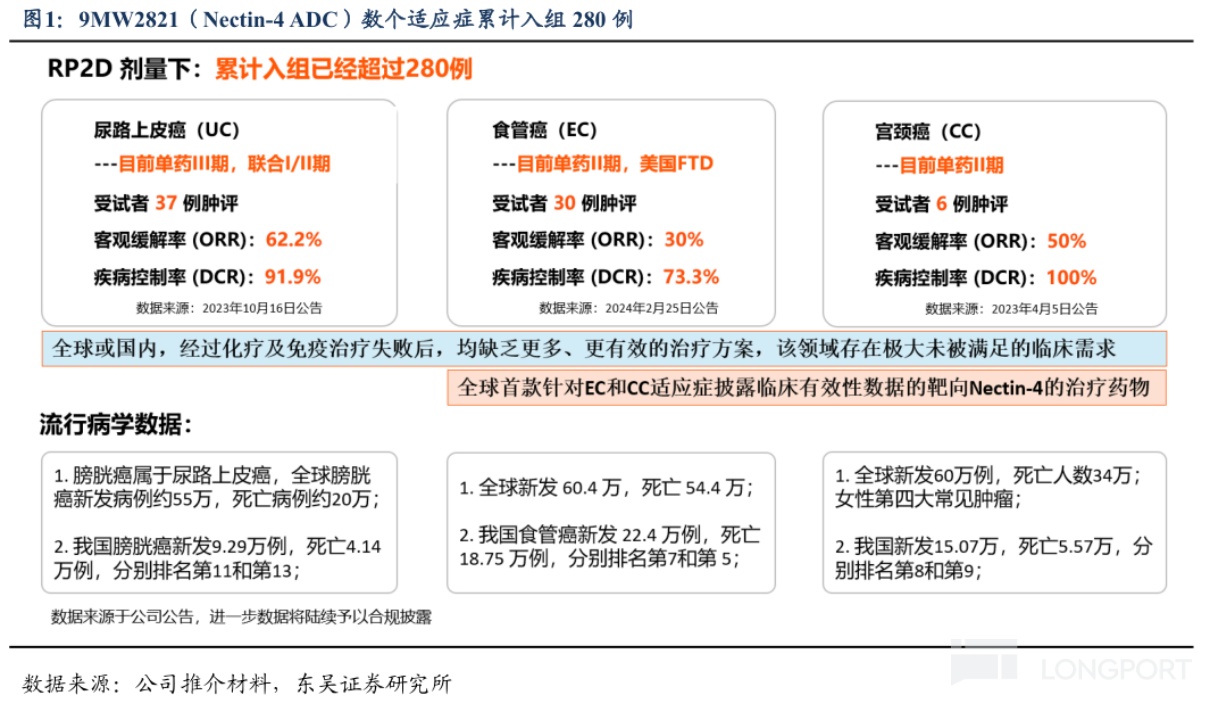
9MW2821 是国内首个开展临床试验的 Nectin-4 ADC,进度处全球第二,适应症为晚期实体瘤:尿路上皮癌已处于Ⅲ期,宫颈癌和食管癌已处于Ⅱ期,并已读出积极数据。
其中,针对宫颈癌,37 例可评估疗效的患者 ORR、DCR 分别为 40.54%、89.19%;单药治疗晚期尿路上皮癌患者的 ORR、DCR 分别为 62.2%、91.9%,中位 PFS 为 6.7 个月;针对食管癌,单药治疗并完成一次肿评的 30 例晚期食管癌患者的 ORR、DCR 分别为 30%、73.3%。
值得一提的是,全球首款 Nectin-4 ADC 药物Padcev(Enfortumab Vedotin)2023 年销售额达 556 亿日元(约 10.3 亿美元),同比增长 68.1%,上市仅 4 年就跻身 “重磅炸弹药物”。据 Evaluate Pharma 预测,到 2028 年 Padcev 销售额预计将达到 47 亿美元。足见 Nectin-4 ADC 赛道的市场潜力。
7MW3711是基于新型抗体偶联技术平台 IDDCTM 开发的靶向 B7-H3 的 ADC 药物,展现出优于第一三共 DS7300 的旁观者杀伤效应,在多个 CDX 和 PDX 模型中有良好的体内活性,目前正在开展用于晚期恶性实体瘤的 I/Ⅱ期临床研究。
作为下一代 ADC 药物,B7-H3 ADC 备受外资巨头青睐。
2023 年 10 月,默沙东斥资 220 亿美元交易总额与第一三共达成 3 款 DXd ADC 候选药物的授权交易,其中就包括靶向 B7-H3 的 ADC;紧接着 12 月,葛兰素史克(GSK)以 17.1 亿美元交易总额引进了翰森制药 B7-H3 ADC 药物 HS-20093 在大中华区以外的全球权益。
9MW1911是针对 IL33/ST2 通路的创新单抗,开发适应症包括哮喘、慢性阻塞性肺疾病(COPD)和特应性皮炎等,其中 COPD 已处于临床 Ib/IIa 期。目前全球尚无以 ST2 或其配体 IL-33 为靶点的抗体药物上市,9MW1911 为国内首个进入临床阶段,进度处全球第二梯队。
9MW3811为靶向人白介素-11(IL-11)的人源化单克隆抗体,适应症为晚期恶性肿瘤和特发性肺纤维化,正在中国、澳大利亚和美国开展临床试验,进度处国内首家、全球第一梯队,而且与 PD-1 抗体联用可表现出更好的抗肿瘤药效。
04
结语
迈威生物的研发布局可谓步步为营、稳扎稳打:先让生物类似药 “出道”,然后巧妙地利用 “出海” 策略,让产品在海外市场崭露头角,同时也为公司注入源源不断的现金流。
如今,迈威生物的多款研发管线已进入临床后期阶段,蓄势待发,尤其是那些创新度高、差异化优势显著的 ADC 管线,仿佛就是为 “出海” 而生。
回想去年那些通过产品授权 “出海” 而首次实现盈利的 Biotech,不知道迈威生物会不会成为下一个?
参考资料:
1.迈威生物财报、公告、官微
2.国信证券、德邦证券、东吴证券研报
$迈威生物-U.SH $博安生物.HK $石药集团.HK